
Composition chimique Purate™
Particularités du produit
Comment le ClO2 se compare-t-il aux autres technologies?
Le dioxyde de chlore (ClO2) est une molécule remarquable assurant de bonnes performances comparativement aux autres technologies.
Dioxyde de chlore vs chlore
Les préoccupations en matière de sécurité soulevées par le chlore gazeux ont poussé de nombreux utilisateurs à changer pour des produits comme le dioxyde de chlore (ClO2).
Le chlore, comme le chlore gazeux ou l'hypochlorite de sodium, est utilisé depuis des années comme préoxydant et désinfectant principal. Toutefois, son utilisation diminue en raison des problèmes associés à la formation de sous-produits préoccupants. Le chlore est un antimicrobien plus faible que le ClO2, surtout à un pH de plus de 7. Bien que le chlore soit généralement meilleur marché par unité de poids, les coûts de traitement totaux sont souvent inférieurs avec du ClO2 en raison de son efficacité accrue. Le chlore peut entraîner des odeurs problématiques, alors que le ClO2 peut résoudre les problèmes d'odeur et de goût.
Parce que le ClO2 produit moins de sous-produits préoccupants, il est souvent utilisé au début dans des installations de traitement de l'eau comme préoxydant, souvent pour le contrôle du Fe et du Mn.
Dioxyde de chlore versus ozone
Le fort potentiel oxydant de l'ozone mène à la formation de bromate, un cancérogène réglementé trouvé dans l'eau potable.
L'ozone est un antimicrobien plus puissant que le ClO2. Toutefois, dans les sources d'eau contenant du bromure, la dose d'ozone acceptable peut être sévèrement limitée par les limites en matière de bromate. En raison de la haute réactivité de l'ozone, tout résidu n'a qu'une courte durée de vie et s'avère difficile à mesurer. De plus, les coûts d'exploitation et d'entretien des systèmes à ozone sont élevés.
Les systèmes à dioxyde de chlore coûtent beaucoup moins cher à installer.
Dioxyde de chlore versus UV
Un traitement final aux UV combiné à un prétraitement au dioxyde de chlore (ClO2) peut constituer une solution de traitement de l'eau très efficace.
Les UV et le ClO2 nécessitent tous les deux des contacts de courte durée pour l'inactivation des micro-organismes. Ils ne sont pas affectés par l'ammoniac présent dans l'eau. Les systèmes à UV coûtent cher à installer, à exploiter et à entretenir. Une source d'alimentation de secours est souvent de mise pour un système à UV, ce qui ajoute considérablement aux coûts en raison de la forte demande en électricité.
Parce que le traitement aux UV ne fournit aucun désinfectant résiduel, un essai bactériologique est requis pour en déterminer l'efficacité, ce qui nécessite plus de 24 heures.
Nom : Dioxyde de chlore
Synonymes : « Chlo-2 », oxyde de chlore, peroxyde de chlore
Formule : ClO2
Poids moléculaire : 67,4518
Numéro CAS : 10049-04-4
Angle de liaison : 117,5°
Longueur de liaison : 0,147 nm
Moment dipolaire :5,95 x 10-30 C*m
Facteur acentrique : 0,35638
Structure :


| Variables d'état | Propriétés thermiques |
|---|---|
| Apparence : Gaz jaune-vert à orange-rouge, solide cristallin rouge. | Chaleur de formation : 24,50 kcal/mole |
| Expédition habituelle : Produit sur place; expédition non permise | Énergie de Gibbs : 28,80 kcal/mole |
| Point de fusion/congélation : -59,5 °C (-75,1 °F) | Entropie du gaz parfait : 0,257 kJ/mole K |
| Point d'ébullition : 10,9 °C (51,6 °F) à 760 mm Hg 9,9 °C (49,8 °F) à 731 mm Hg |
Puissance calorique nette (gaz) : -24,50 kcal/mole |
| Température critique : 192 °C (377,6 °F) | Chaleur de dissolution dans l'eau : 6,6 kcal/mole |
| Pression critique : 8621,6 kPa (1250,6 lb/po²) | Volume molaire liquide : 4,1852 x 10 à 2 m3/kmol |
| Température du point triple : -59,5 °C (-75,1 °F) |
Pression du point triple : 1,2544 kPa (9,4 mm Hg abs.) |
| Densités | Température/variables dépendantes |
|---|---|
| Liquide : 1,773 g/mL à -55 °C 1,640 g/mL à 0 °C 1,614 g/mL à 10 °C |
Capacité calorifique du gaz : 0,0408 kJ/(mole K) à 0 °C 0,0417 kJ/(mole K) à 20 °C 0,0425 kJ/(mole K) à 40 °C |
| Gaz : 3,09 g/l à 11 °C | Chaleur de vaporisation : 26,937 kJ/mole à 0 °C 25,825 kJ/mole à 20 °C 24,629 kJ/mole à 40 °C |
Pour tous les chimistes et ingénieurs dans la salle, on retourne à la classification périodique des éléments et à la stœchiométrie.
PURATE – Haute efficacité
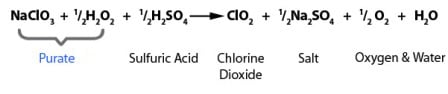
La composition chimique PURATE avec ClO2 fait ressortir la réduction du chlorate de sodium avec le peroxyde d'hydrogène dans des conditions acides de manière à produire du dioxyde de chlore (ClO2). Notre solution PURATE prémélangée vous simplifie la tâche.
Concurrents – Faible efficacité
L'efficacité de certains générateurs à base de chlorite peut atteindre 95 % lorsqu'ils sont adéquatement calibrés. Toutefois, le rendement des générateurs à trois produits chimiques (chlorite de sodium + hypochlorite + HCl) diminue rapidement et de tels générateurs nécessitent des calibrations et des ajustements fréquents. Leur efficacité s'en trouve par conséquent le plus souvent réduite.
Une technologie de chlorite en particulier (chlorite de sodium + HCl) présente une grande efficacité, mais un faible rendement. Le besoin d'utiliser 5 molécules de chlorite de sodium pour produire 4 molécules de ClO2 est inhérent à la composition chimique, pour un rendement maximum possible de 80 %. En raison d'un faible rendement, cette technologie est économiquement limitée à de petits comptes, habituellement de moins de 1 kg/h.
![]()
Le dioxyde de chlore produit par PURATE est accepté dans le monde entier, certifié par CE (équipement seulement), enregistré auprès de l'EPA, approuvé par la FDA et le BfR, certifié kascher (OU) et certifié NSF 60 (équipement/précurseur).
PURATE et l'acide sulfurique NE sont PAS des produits chimiques couverts dans le cadre de la gestion de la sécurité des procédés. Même si le ClO2 est un produit chimique couvert, il est généré sur place et utilisé immédiatement, de façon à ce qu'on ne s'approche jamais ne serait-ce qu'un tant soit peu de la quantité seuil.
Le ClO2 produit par PURATE permet de satisfaire à toutes les exigences des programmes de gestion de la sécurité des procédés et de gestion des risques et d'éviter les coûts associés.


